【2.1.1.1】基于mRNA的疗法-开发新型药物
- Messenger RNA(mRNA)是生命的关键分子,几乎涉及细胞生物学的所有方面。
- 作为基础研究和应用研究的主题已有5多年的历史,mRNA作为具有潜在强大功能的能够传递遗传信息的药物,直到最近才成为人们关注的焦点。
- 合成的mRNA可以被改造成类似于成熟的和经过加工的mRNA分子,因为它们天然存在于真核细胞的细胞质中并可以瞬时递送蛋白质。
- 最新进展解决了此类药物固有的挑战,并为广泛的应用奠定了基础
- 除了癌症免疫疗法和传染性疾病疫苗以外,新的方法,例如体内递送mRNA以替代或补充蛋白质,基于mRNA的多能干细胞诱导或用于基因组工程的mRNA辅助设计核酸酶的递送,都迅速出现并进入了药物开发。
这篇综述全面综述了mRNA药物技术的现状,其应用以及与基于mRNA的药物发现和开发有关的关键方面。
摘要:
体外转录(IVT,In vitro transcribed)mRNA最近已成为一种潜在的传递遗传信息的新药,成为人们关注的焦点。此类合成的mRNA可通过在结构上类似于天然mRNA的方法进行工程改造,以瞬时表达蛋白质。解决此类药物固有挑战的进展,特别是与控制IVTmRNA的翻译功效和免疫原性有关的进展,为广泛的潜在应用提供了基础。基于mRNA的癌症免疫疗法和传染性疾病疫苗已进入临床开发。同时,新兴的新方法包括体内提供IVT mRNA来替代或补充蛋白质,使用IVT mRNA编码的设计者核酸酶,基于IVT mRNA的多能干细胞生成和基因组工程设计。这篇综述全面概述了基于mRNA的药物技术及其应用的现状,并讨论了将这些技术发展为新型药物的主要挑战和机遇。
一、主要
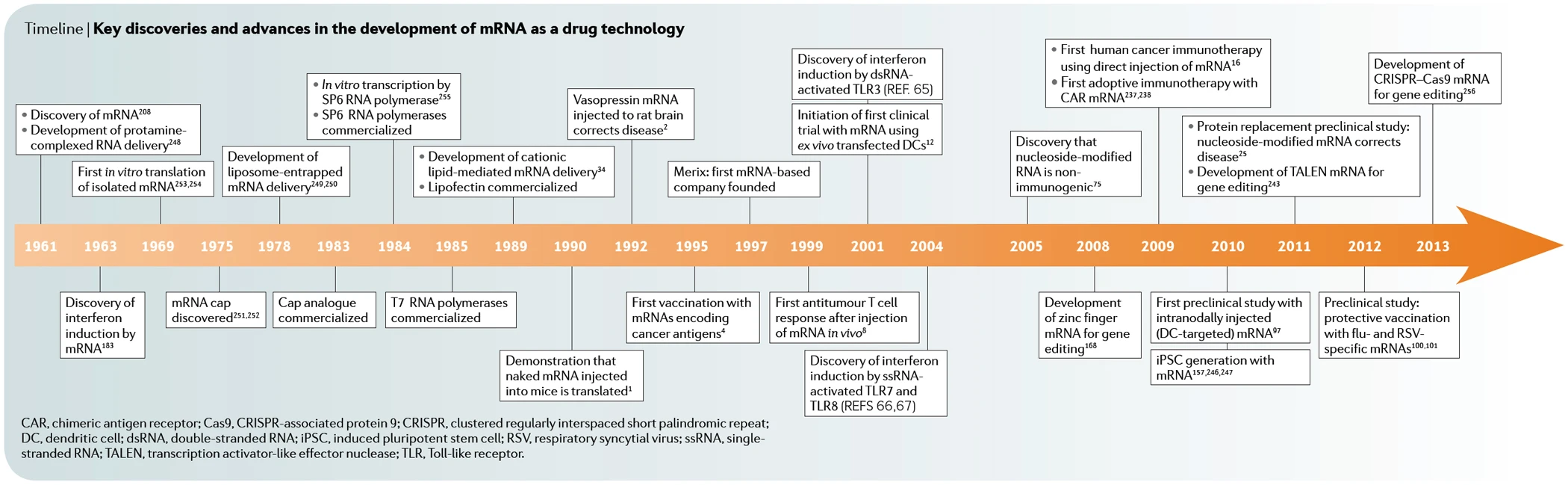
核酸编码药物的概念是在二十多年前Wolff等人提出的。图1证明了将体外转录的(IVT)mRNA或质粒DNA(pDNA)直接注射到小鼠的骨骼肌中导致了所编码的蛋白质在所注射的肌肉中的表达。当时,由于其不如DNA稳定,因此不再追求mRNA,因此该领域专注于基于pDNA和病毒DNA的技术。然而,自1961年被发现以来,mRNA一直是各种疾病的持续基础和应用研究的主题(图1(时间线))。发现真核细胞后的最初几十年,重点是了解mRNA的结构和功能方面及其在真核细胞中的代谢。这是使mRNA重组工程工具更广泛的研究团体所能用的。在20世纪90年代,IVT mRNA的临床前勘探已启动用于各种应用,包括蛋白质置换和疫苗接种方法对癌症和传染病。因此,积累的知识使最近的科学和技术进步克服了与mRNA相关的一些障碍,例如半衰期短和免疫原性差。
从概念上讲,基于IVT mRNA的治疗方法与其他基于核酸的治疗方法之间存在几个重要区别。
- IVT mRNA无需进入细胞核即可发挥功能。一旦到达细胞质,mRNA即刻翻译。相比之下,DNA治疗剂需要进入细胞核才能转录成RNA,其功能取决于细胞分裂过程中核被膜的分解。
- 另外,不同于质粒DNA和病毒载体,基于IVT mRNA的治疗剂不整合到基因组中,因此不存在插入诱变的风险。对于大多数药物应用而言,IVT mRNA仅具有瞬时活性,并通过生理代谢途径完全降解也是有利的。。
在治疗性癌症疫苗的领域中,IVT mRNA的经历广泛的临床前调查和已达到III期临床试验。在其它领域,如蛋白质-替代疗法肿瘤学,心脏病学,内分泌学,血液学,肺药或其它疾病的治疗,基于基因-IVT治疗的发展正处于临床前研究阶段。为了推进蛋白质替代疗法,需要解决诸如mRNA的靶向递送及其复杂药理学之类的未解决的问题。
在这里,我们提供了基于mRNA的药物技术及其各种应用的当前状态的全面概述。我们讨论基于mRNA的疗法的生物药物开发的特殊性,以及可能影响该药物类别进展的优势和关键挑战。
方框1:对mRNA的学术和工业兴趣
最近,几所大学开设了RNA中心,以促进RNA的治疗应用,包括体外转录(IVT)mRNA。这些中心包括美国马萨诸塞州大学的RNA治疗研究所,美国耶鲁大学RNA科学和医学中心以及美国纽约州立大学奥尔巴尼大学的RNA研究所。大学衍生公司(例如Argos Therapeutics,BioNTech,CureVac,eTheRNA,Ethris,Factor Bioscience,Moderna和Onkaido)也加快了基于mRNA的疗法的临床前和临床开发。
诺华,赛诺菲巴斯德,阿斯利康,Alexion和Shire等主要制药公司已开始开发基于mRNA的产品。IVT mRNA技术正在获得许可(例如,2013年,阿斯利康与Moderna达成的2.4亿美元交易,2014年与Curevac达成的Sanofi Pasteur交易,2013年与Ethris的Shire合作,以及Moderna与2014年的Alexion;有关更多信息,请参见FierceBiotech网站。2013年10月,第一届国际mRNA健康大会在德国历史名城图宾根举行,在140年前就发现了核酸207
二、mRNA药理学的主要概念
使用IVT mRNA作为药物的背后概念是将确定的遗传信息转移到患者的细胞中,以达到预防或改变特定疾病状态的最终目的。
原则上,正在寻求使用IVT mRNA的两种方法。
- 一种是将其离体转移到患者的细胞中。然后将这些转染的细胞过继给药给患者。目前正在研究此方法用于基因组工程,基因重编程,基于T细胞和树突状细胞(DC)的免疫疗法来治疗癌症和传染病,以及一些蛋白质替代方法。
- 第二种方法是使用各种途径直接递送IVT mRNA。正在开发此方法,以用于肿瘤学和传染病,用于治疗过敏的耐受方案以及其他蛋白质替代疗法。
对于离体转染和直接疫苗接种,mRNA药理学的以下一般原则适用。
转染细胞的机制用于将信息体内翻译为相应的蛋白质,该蛋白质是药理活性产品。因此,编码治疗性蛋白质的mRNA与抑制蛋白质表达的小干扰RNA(siRNA)的作用相反。IVT mRNA被设计成在结构上类似于真核细胞胞质中天然存在的成熟和加工过的mRNA。因此,IVT mRNA是单链的,具有5’帽和3’poly(A)尾巴。编码目标蛋白质的开放阅读框(ORF)以起始密码子和终止密码子标记,并以非翻译区(UTR)为侧翼。
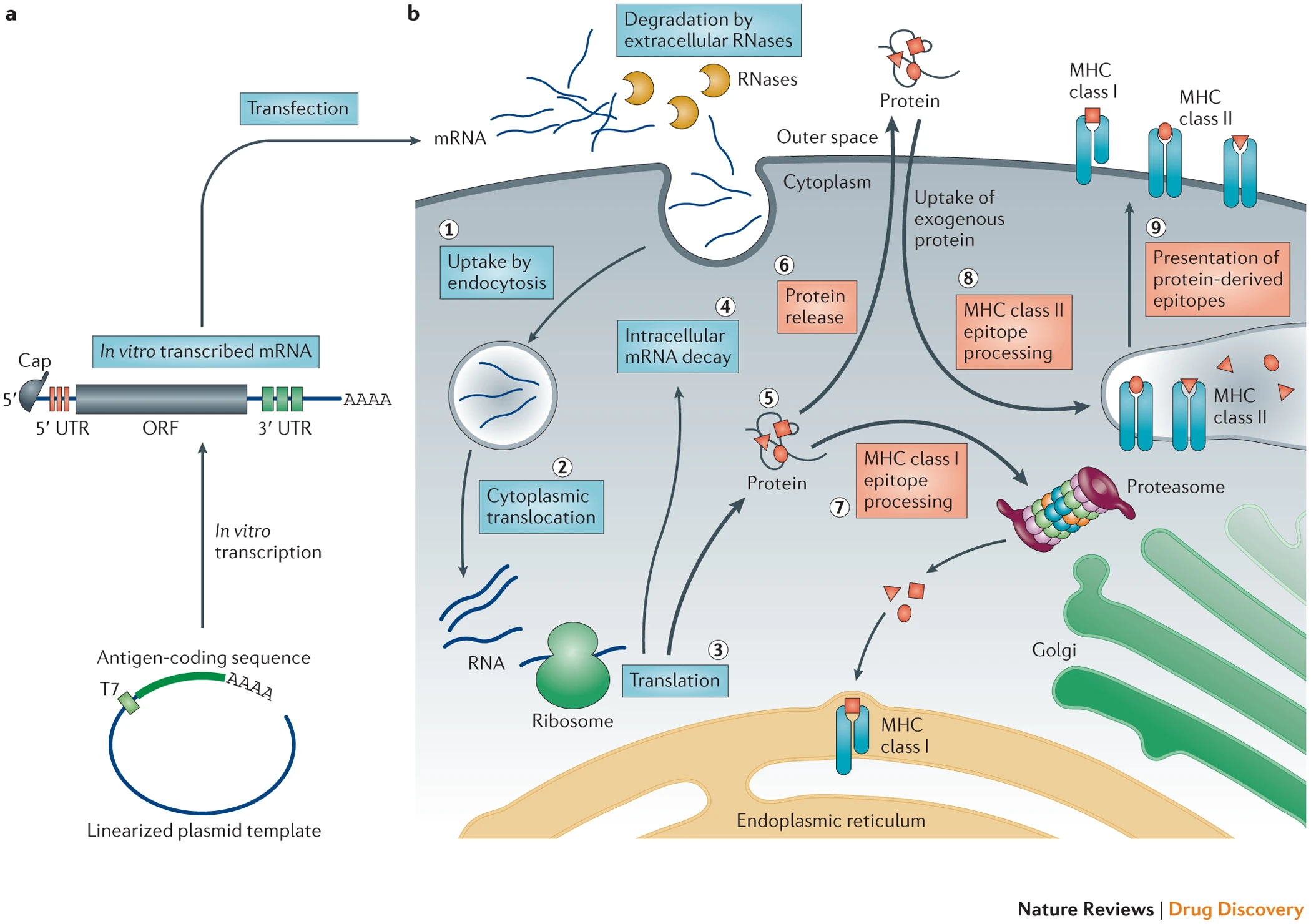
图2 a) 一个具有抗原编码序列的线性化DNA质粒模板用于体外转录。在体外转录的mRNA中包含的帽,5’和3’非翻译区(UTR),开放阅读框(ORF)和聚(A)尾,这决定了其转移入后的mRNA分子的翻译活性和稳定性细胞。b) 步骤1:一部分外源mRNA通过普遍存在的RNase逃脱降解,并通过细胞特异性机制(例如,未成熟树突状细胞中的巨胞饮作用)自发内吞并进入内体途径。步骤2:尚未完全了解mRNA在细胞质中的释放机制。步骤3:mRNA的翻译使用宿主细胞的蛋白质合成机制。mRNA翻译的限速步骤是真核翻译起始因子4E(eIF4E的)与帽结构的结合。mRNA与核糖体,真核起始因子eIF4E和eIF4G以及poly(A)结合蛋白的结合导致形成环状结构和主动翻译。步骤4:通过mRNA的降解翻译终止是通过外切核酸酶催化的。盖子被清除剂去盖酶DCP1,DCP2和DCPS 水解,然后用5'–3’外切核糖核酸酶1(XRN1)消化残留的mRNA。如果mRNA沉默并且驻留在细胞质加工体中,则降解可以被延迟。可替代地,可能发生在外来体mRNA的核酸内切裂解。异常mRNA(例如,具有过早终止密码子的mRNA)的分解代谢受各种其他机制控制。步骤5:翻译的蛋白质产物经历翻译后修饰,其性质取决于宿主细胞的性质。然后,翻译的蛋白质可以在已产生蛋白质的细胞中起作用。步骤6:或者,蛋白质产物被分泌并且可以通过自分泌,旁分泌或内分泌机制起作用。步骤7:为了免疫治疗使用mRNA,需要将蛋白质产物降解为抗原肽表位。这些肽表位被加载到主要的组织相容性复合物(MHC)分子上,从而确保这些抗原向免疫效应细胞的表面呈递。细胞质蛋白被蛋白酶体降解并被转移到内质网,在那里它们被装载在I类MHC分子上并呈递给CD8 +细胞毒性T淋巴细胞。MHC I类分子几乎由所有细胞表达。步骤8:在抗原呈递细胞中,为了获得同源的T细胞帮助以实现更有效和可持续的免疫反应,需要将蛋白质产品送至MHC II类装载区室。这可以通过将路由信号编码序列并入mRNA中来完成。此外,树突状细胞吸收的外源抗原也可以通过一种称为交叉引物的机制进行处理并加载到I类MHC分子上。步骤9:然后,MHC I类和MHC II类分子可以将蛋白质衍生的抗原决定簇呈递到细胞表面。
通过从DNA模板(例如线性化质粒或PCR产物)进行体外转录,在无细胞系统中合成mRNA 。除5’帽外,此DNA模板编码功能性mRNA的所有结构元件。在核苷酸存在的情况下,用T7或SP6 RNA聚合酶进行体外转录,然后将mRNA酶促封端。然后通过DNA酶消化模板DNA,并通过常规使用的分离核酸的方法纯化mRNA。
IVT mRNA的药效学活性的主要部分是细胞质。与在细胞核中产生并通过核输出进入细胞质的天然mRNA相反,IVT mRNA必须从细胞外空间进入细胞质。
无论IVT mRNA是在体外还是在体内递送到细胞,两个关键因素决定了其细胞质的生物利用度。
- 一种是被高度活跃的普遍存在的RNase迅速降解,这种酶在细胞外空间中很丰富。
- 另一个是细胞膜,它会阻止带负电荷的大mRNA分子被动扩散到细胞质中。原则上,真核细胞能够主动吞噬裸露的mRNA。然而,在大多数细胞类型中,摄取率和细胞质转移是最小的(少于最初的mRNA输入的10,000个分子中的1个)。可以通过将IVT mRNA与络合剂一起配制来改善细胞的转染,络合剂可以保护mRNA不受RNase降解,还可以促进细胞摄取。或者,可以使用无核糖核酸缓冲液中的电穿孔等技术有效地进行离体 mRNA转移到细胞中。
IVT mRNA一旦进入细胞质,其药理作用就由调节天然mRNA稳定性和翻译的复杂细胞机制所决定。
从IVT mRNA转录的蛋白质产物经过翻译后修饰,该蛋白质是生物活性化合物。IVT mRNA模板和蛋白质产物的半衰期是基于mRNA的治疗药物药代动力学的关键决定因素。
一旦产生了编码的蛋白质,其目的地就由信号肽确定。这些可以是天然蛋白质序列所固有的,也可以是重组工程以将蛋白质导向宿主细胞内所需的细胞区室。或者,可以分泌蛋白质以作用于邻近细胞,或者如果释放到血流中,则作用于遥远的器官。
对于免疫治疗方法,编码蛋白的加工途径对于确定其药效学至关重要。与内源性蛋白质的命运相似,mRNA编码的产物被蛋白酶体降解,并在主要的组织相容性复合体(MHC)I类分子上呈递给CD8 + T细胞。通常,细胞内蛋白未达到II类MHC加工途径来诱导T辅助细胞应答。但是,通过将分泌信号引入抗原编码序列,可以实现T辅助细胞反应,因为分泌信号将蛋白质抗原重定向到细胞外空间。
三、改善mRNA的翻译和稳定性
治疗效果所需的IVT mRNA量和治疗持续时间取决于许多因素。这些包括编码蛋白的预期生物学功能及其作用方式,以及蛋白的效价和循环半衰期,对于不同的应用,其变化幅度可能会达到几个数量级。纳克级至微克级的高抗原蛋白可能足以有效诱导人的免疫反应。相反,递送全身活性生长因子,激素或单克隆抗体可能需要毫克或什至克量的蛋白质。通过迭代优化IVT mRNA的翻译能力和细胞内稳定性,每单位mRNA可以生成的蛋白质量已大大增加。
已投入大量精力来修饰IVT mRNA的结构元件-特别是5’cap,5'-和3'-UTR,编码区和poly(A)尾巴-以系统地改善其细胞内稳定性和翻译效率(图3)。这些改进最终导致在更长的时间范围内产生大量的编码蛋白。从到超过1周的范围内的几分钟。尚未充分探讨调节mRNA药理学的机会范围,对mRNA结合因子及其结合位点的更深入了解可能为工程化具有多种药代动力学特性的mRNA载体提供更多机会。
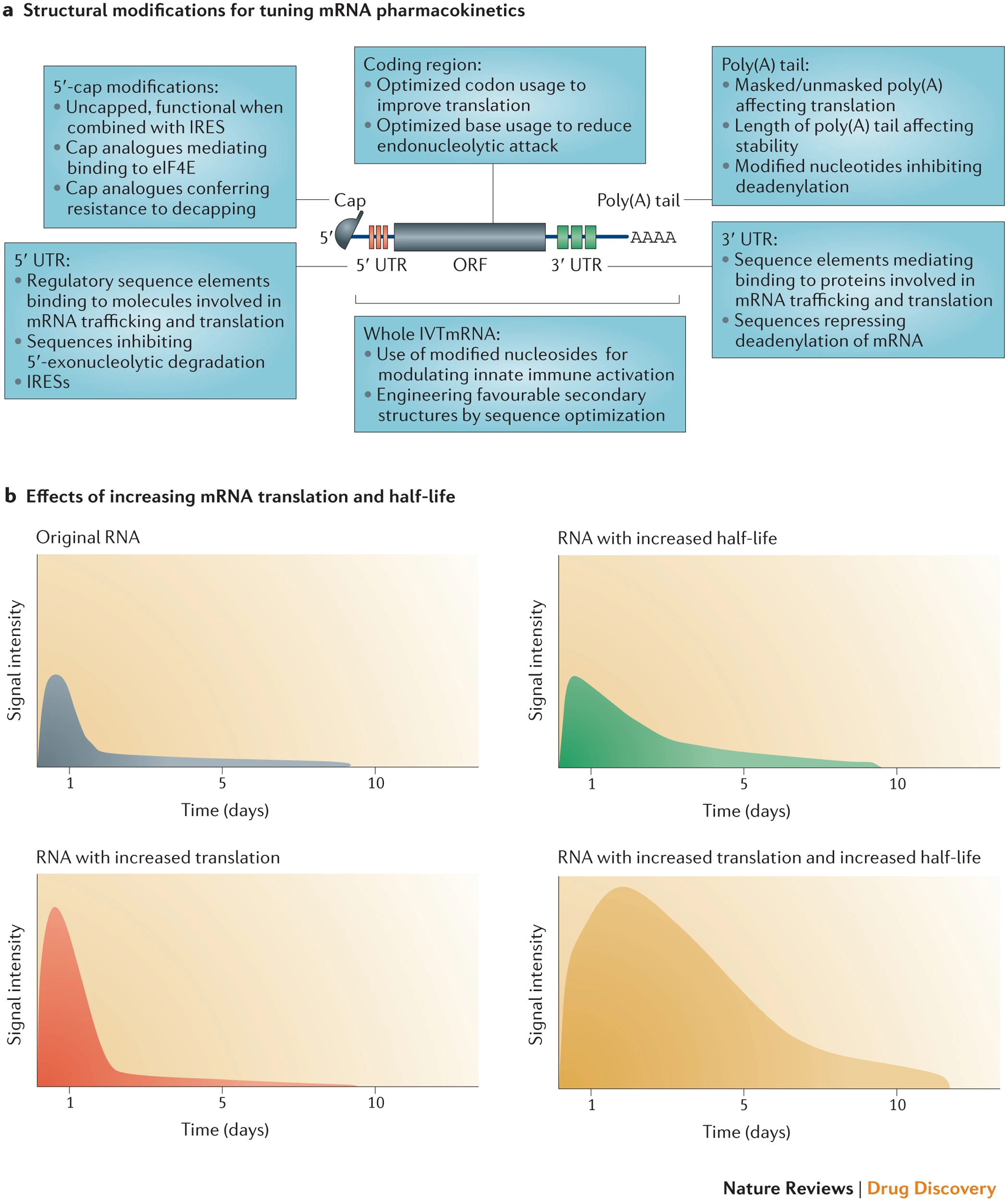
a) 体外转录(IVT)mRNA的关键结构要素及其修饰策略。b ) 取决于单独使用或结合使用哪些元素(例如,修饰帽,非翻译区(UTR)或poly(A)尾巴),可以调节和微调蛋白产物表达的持续时间和动力学特征。eIF4E,真核翻译起始因子4E;IRES,内部核糖体进入位点;ORF,打开阅读框。
3.1 The 5′ cap 5’帽
mRNA的可靠翻译需要功能性的5’帽结构。天然的真核mRNA具有一个7-甲基鸟苷(m 7 G)帽,在转录过程中通过5'-5'-三磷酸桥(ppp)(m 7 GpppN结构)与该mRNA连接。5’帽与真核翻译起始因子4E(EIF4E)的结合对于有效翻译至关重要,而其与mRNA降解酶DCP1,DCP2或DCPS的结合则可调节mRNA的降解。在IVT mRNA初始合成后对其加帽的一种方法是使用重组牛痘病毒衍生的加帽酶进行第二步。所得的帽结构与最常见的天然真核帽结构相同。另一种更常用的方法是将合成的帽类似物添加到体外转录反应中,并在一个步骤中进行加帽和体外转录。但是,这种方法的主要局限性是帽转录类似物和体外转录所需的GTP核苷酸竞争,导致某些mRNA保持未加帽且翻译无活性。
用包含产生IVT的mRNA进行早期的mRNA研究m7 GpppG帽类似物,而大部分的正在进行的临床试验仍然使用这种类型的mRNA。然而,大量的m 7 GpppG类似物以相反的方向掺入mRNA中,因此未被翻译机制识别,从而导致较低的翻译活性。因此,所谓的防反转帽类似物(ARCAS;米2 7,3'-O GpppG)引入。ARCA-帽mRNA在多种细胞类型表现出优异的翻译效率。最近,开发了含硫代磷酸酯的ARCA cap类似物。该帽类似物赋予了对DCP2脱盖的抗性,从而进一步延长了mRNA 的半衰期。在小鼠中进行的实验表明,含有硫代磷酸酯修饰的帽的IVT mRNA可以诱导针对编码蛋白的强力免疫反应,并且该反应要强于带有对照帽的mRNA所诱导的反应。帽类似物对IVT mRNA的翻译和稳定性的影响似乎取决于细胞类型和细胞分化状态。
3.2 聚(A)尾巴 The poly(A) tail
poly(A)尾部与5’帽,内部核糖体进入位点和各种其他决定因素协同作用,调节mRNA的稳定性和翻译效率。通过在转录的模板载体中编码poly(A)片段或通过使用重组poly(A)聚合酶以酶促方式扩展IVT mRNA的两步反应,可将IVT mRNA拖尾。重组聚(A)聚合酶能够将修饰的核苷酸掺入到聚(A)尾部,从而抑制聚(A)特异性核酸酶引起的腺苷酸化。已针对各种核苷类似物(包括虫草素(3'-脱氧腺苷) )探索了这种方法。然而,虫草素不能增加mRNA的半衰期。失败的原因很可能是虫草素是链终止剂,因此仅在最终的3’位置掺入。
酶促聚腺苷酸化的局限性在于,每种RNA制剂均由多聚腺苷酸尾巴长度不同的RNA种类的混合物组成。相反,从DNA模板体外转录RNA会产生具有确定的poly(A)尾部长度的RNA,因此是优选的,特别是在mRNA打算用于临床应用的情况下。DC中的分析表明,该聚(A)尾的3’端不应该由附加的碱基和该聚(A)尾的最佳长度是120和核苷酸150之间被掩蔽
3.3 5'-和3'-UTR 5′- and 3′-UTRs
优化细胞中IVT mRNA的翻译和稳定性的另一种策略是掺入含有调节序列元件的5'-和3'-UTR,所述调节序列元件已被鉴定为调节内源性mRNA的翻译和稳定性。
例如,许多IVT的mRNA含有窝藏增加mRNA的稳定性和翻译几个序列元件α-和β珠蛋白mRNA的3'-UTR的。人β球蛋白序列的-UTR -3'-的稳定作用是通过使用两个人β珠蛋白3'-UTR的布置在头-尾方向进一步增强。另外,细胞和病毒5'-和3'-UTR的各个区域增强了mRNA的稳定性和翻译效率。例如,许多正痘病毒mRNA中存在的真核生物延伸因子1α(EEF1A1)mRNA 的3'-UTR和5'-UTR元件既抑制去盖化也抑制3'-5’核酸外切降解(参见参考文献48))。对于某些应用,可能需要使mRNA不稳定来限制蛋白质生产的持续时间。可以通过将富含AU的元素掺入3'-UTRs中来实现此效果,从而确保mRNA迅速降解和较短的蛋白质表达时间
3.4 编码区域 The coding region
已知密码子组成会影响翻译效率。用同义的频繁密码子替换稀有密码子可提高翻译产量,因为由于核糖体附近tRNA的氨基酰化,相同tRNA的重用可加速翻译。密码子上下文(即,邻近的核苷酸和密码子)也影响翻译延伸率和翻译效率。类似于基于重组DNA的方法(在参考文献53中进行了综述),密码子优化的IVT mRNA已成功用于抗病毒感染的疫苗研究和非病毒蛋白的表达。
但是,可能有正当的理由避免使用优化的密码子。一些蛋白质需要缓慢的翻译,这需要稀有的密码子才能保证它们正确折叠。对于某些IVT mRNA编码的疫苗而言,维持原始ORF也可能是有益的。当IVT mRNA的由于不同的帧被转换可以产生有力的隐蔽性T细胞表位的核糖体框架移或平移时被启动的内部或从CUG起始密码子。密码子优化应消除抗原肽的这些重要来源。
三、IVT mRNA的免疫刺激活性
对于接种,IVT mRNA的强免疫刺激效应,固有的佐剂活性的增加的好处,并导致有效的抗原特异性细胞和体液免疫应答。类型的免疫应答的似乎取决于一系列因素,包括在其中的mRNA IVT掺入颗粒的类型和尺寸的特征。但是,在诸如蛋白质替代疗法的应用中,IVT mRNA激活先天免疫系统是一个主要缺点。鉴定细胞中RNA传感器和mRNA中涉及免疫识别的结构元件的最新进展提供了通过IVT mRNA增强免疫激活或根据需要创建“去免疫” mRNA的机会。
IVT mRNA通过激活模式识别受体来诱导免疫刺激,其自然作用是通过诱导各种下游效应来识别和响应病毒RNA(图4)。
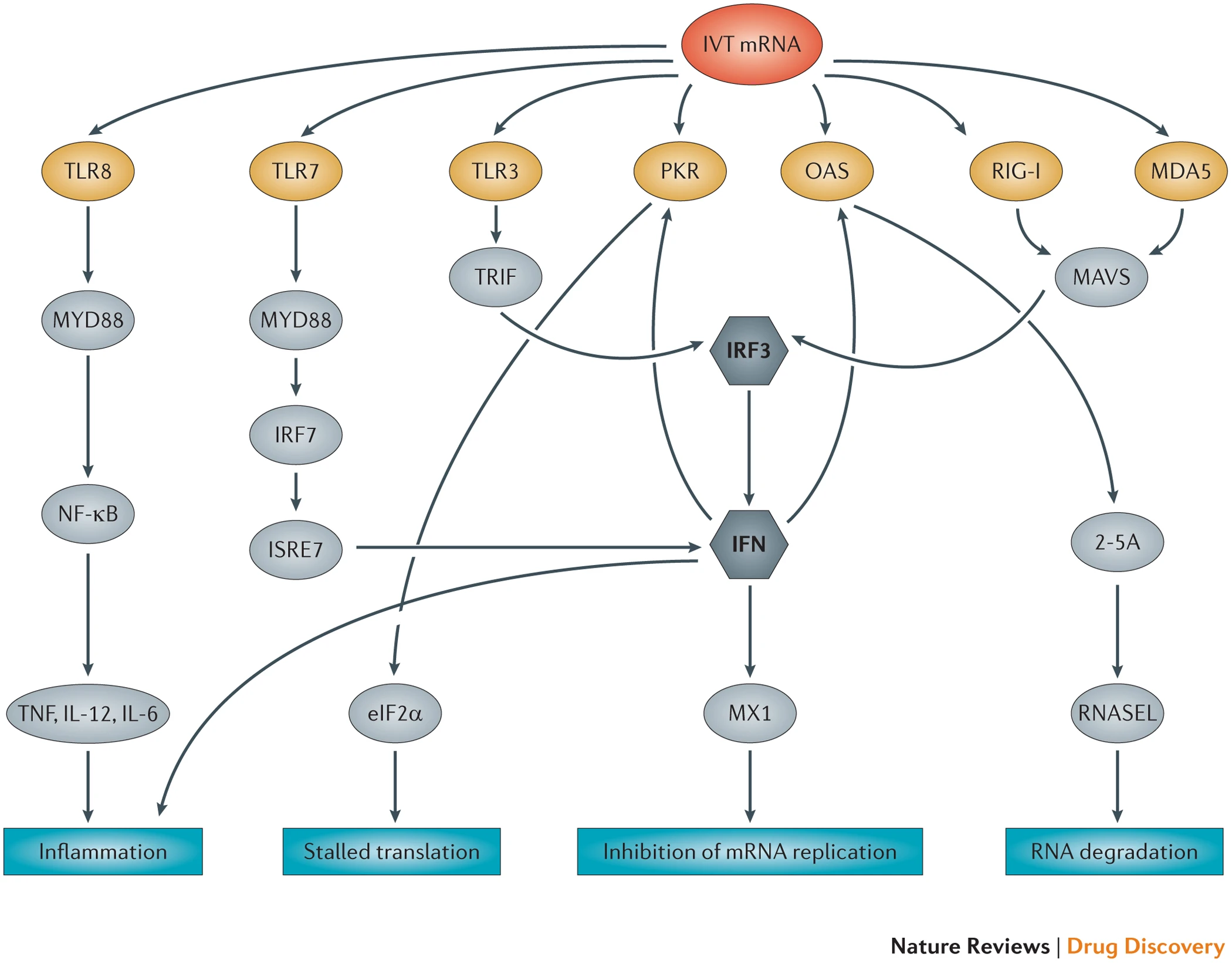
图4 体外转录的(IVT)mRNA被多种内体先天免疫受体(Toll样受体3(TLR3),TLR7和TLR8)和细胞质先天免疫受体(蛋白激酶RNA激活(PKR),视黄酸诱导基因I蛋白( RIG-I),黑色素瘤分化相关蛋白5(MDA5)和2'-5'-寡腺苷酸合酶(OAS))。通过这些不同途径的信号转导导致与1型干扰素(IFN),肿瘤坏死因子(TNF),白介素6(IL-6),IL-12相关的炎症以及转录程序级联的激活。总体而言,它们创造了一种诱发特定免疫反应的促炎性微环境。此外,下游效应,例如由于真核翻译起始因子2α(eIF2α)磷酸化而导致的翻译减慢,核糖核酸酶L(RNASEL)的过表达增强了RNA的降解并抑制了自我扩增mRNA的复制,这与IVT mRNA的药代动力学和药效学有关。IRF,干扰素调节因子;ISRE7,干扰素刺激的反应元件;MAVS,线粒体抗病毒信号蛋白;MDA5,黑色素瘤分化相关蛋白5;MYD88,髓样分化初级反应蛋白88;MX1,粘液病毒(流感)耐药性1;NF-κB,核因子-κB;TRIF,含有Toll-IL-1受体域的衔接子蛋白,可诱导IFNβ。线粒体抗病毒信号蛋白;MDA5,黑色素瘤分化相关蛋白5;MYD88,髓样分化初级反应蛋白88;MX1,粘液病毒(流感)耐药性1;NF-κB,核因子-κB;TRIF,含有Toll-IL-1受体域的衔接子蛋白,可诱导IFNβ。线粒体抗病毒信号蛋白;MDA5,黑色素瘤分化相关蛋白5;MYD88,髓样分化初级反应蛋白88;MX1,粘液病毒(流感)耐药性1;NF-κB,核因子-κB;TRIF,含有Toll-IL-1受体域的衔接子蛋白,可诱导IFNβ。
在免疫细胞中,位于内体区室的Toll样受体TLR3,TLR7和TLR8被内吞的IVT mRNA激活并诱导干扰素分泌。TLR3识别双链RNA(dsRNA的),而TLR7和TLR8正义单链RNA(ssRNA)。聚(U)是最有效的干扰素诱导剂,和通过TLR7(注释作用)。相比之下,在非免疫细胞中,大多数干扰素的产生是通过激活胞质视黄酸诱导基因I蛋白(RIG-I;也称为DDX58)和黑素瘤分化相关蛋白5(MDA5)来激活的。 ;也称为IFIH1)。RIG-1是由短的,双链的,5'-三磷酸的RNA活化,而MDA5响应长dsRNA和病毒mRNA缺乏2'- ø -methylation。
细胞质RNA传感器介导免疫刺激并影响mRNA翻译的效率,最终导致翻译停滞,RNA降解和直接的抗病毒活性(图4)。这些作用部分是由蛋白激酶RNA激活的(PKR;也称为EIF2AK2)介导的,它使真核翻译起始因子2α(eIF2α)磷酸化并最终抑制mRNA翻译。可以通过将天然存在的修饰核苷如假尿苷,2-硫尿苷,5-甲基尿苷,5-甲基胞苷或N6-甲基腺苷掺入到IVT mRNA中来产生去免疫的IVT mRNA。已证明这既可以抑制IVT mRNA的固有佐剂活性,也可以抑制其对翻译的抑制作用。这种修饰的IVT的mRNA出现,以避免TLR7和TLR8(参考文献的活化75),并且其中一些,包括假尿苷和2-硫尿苷的,被示出以使IVT mRNA的检测不到由RIG-I和PKR 。当通过高效液相色谱纯化消除dsRNA污染物(从而消除了所有剩余的TLR3活化)时,修饰的mRNA不再诱导任何免疫刺激作用。假修饰的mRNA的高级翻译已经被归因于其增加的稳定性和结合的降低PKR
四、改善mRNA传递的进展
许多细胞类型可以自发摄取裸露的mRNA。被清道夫受体介导的内吞作用内在化的裸mRNA积累在溶酶体中,只有少量的mRNA泄漏到细胞质中。mRNA释放到细胞质中的机制尚未得到很好的描述,并且在细胞类型之间可能有所不同。此外,mRNA在细胞之间通过外泌体进行交换。在大多数细胞中,mRNA的主动摄取效率很低,并且在低mRNA剂量下会饱和。不成熟的DC专门用于在采样环境时不断吞没细胞外液,这是一个例外,因为它们通过巨胞吞作用吸收mRNA,从而在数个数量级的浓度范围内以线性非饱和方式高效积聚它。结果,为了递送到大多数细胞类型中,需要合适的制剂以保护IVT mRNA免受细胞外RNase介导的降解并促进其进入细胞。
IVT mRNA的传递有两个挑战:
- 一个是达到足够高的编码蛋白净含量,
- 另一个是达到大量细胞。
大多数生理和病理过程,例如细胞迁移,细胞生长,伤口愈合,炎症和血管生成,均由旁分泌信号传导控制。因此,许多预期的临床应用涉及信号分子,例如趋化因子,细胞因子和生长因子,它们被分泌并以旁分泌方式发挥其生物学功能。在这些情况下,总蛋白的量对其生物学效应至关重要。只要释放出足够剂量的编码蛋白并到达其靶细胞,IVT mRNA可以被递送至任何可通过血流或其他途径进入的细胞类型。对于这样的应用,用合成的mRNA转染是合适的方法。对于有效的蛋白激素(例如促红细胞生成素),mRNA的全身递送似乎可导致足够的血浆水平。肝细胞可用于许多类型的聚合物和脂质体递送平台,因此靶向肝脏可能是产生大量重组蛋白的一种方法。
如果要通过IVT mRNA替代缺陷或缺陷的细胞内蛋白,挑战就不同了。在这里,通过IVT mRNA转移恢复的细胞比例必须足够重要才能产生生物学影响。对于此类应用,转染靶细胞的比例而不是绝对蛋白质剂量至关重要。如果将细胞进行离体转染,则对于大多数细胞类型而言,可实现高达80%的细胞转染效率。相比之下,将mRNA体内递送到高比例的确定的靶细胞群中具有挑战性,并且取决于靶细胞的可及性。
4.1 体外转染策略
体外转染策略获得了用IVT mRNA转染的细胞进行过继转移,这得益于制剂的开发,该制剂可保护mRNA免受RNase介导的降解并促进其进入细胞。除各种带正电荷的脂质外,其他含有聚合物的转染剂,例如聚乙烯亚胺,阳离子多肽和树状聚合物(参见参考文献82),可商购。用于体外和体内mRNA递送的mRNA转染试剂盒的数量正在迅速增长。这些进展使使用离体IVT mRNA转染的细胞的临床应用受益。
电穿孔于1982年首次应用于基因转移(参考文献83),现已确立为体外造血造血细胞类型mRNA转染的首选方法。免疫疗法与DC电穿孔与IVT或自体肿瘤来源的mRNA被证明是在癌症患者安全。在阶段IB试验中,患有晚期阶段III和IV期黑素瘤产生强的CD4 +和CD8 +抵抗由IVT的mRNA所编码的抗原的免疫反应。在一项I期试验中,20例转移性前列腺癌患者中有19例也通过发展抗原特异性CD8 + T细胞对治疗产生了反应。在无菌条件下轻柔地电穿孔大量细胞的新型装置的开发,已为广泛的基于IVT mRNA的细胞治疗应用发展了快速的临床级方案
4.2 体内转染策略
临床试验中,裸或鱼精蛋白复合的mRNA的疫苗递送或者皮内ClinicalTrials.gov标识符:NCT01915524和NCT01817738),或直接注射到淋巴结(ClinicalTrials.gov标识符:NCT01684241)正在进行中。但是,尽管裸IVT mRNA的传递似乎足以诱导有效的免疫反应,但对于其他临床应用可能还不够,在这些临床应用中,需要大量大量的蛋白质,而靶向DCs以外的细胞类型。
对于全身递送,基于核酸的药物以纳米级药物制剂的形式给药,并通过开窗或未开窗的毛细血管到达器官。静脉内递送的纳米级载体可进入血流中的细胞,肝细胞以及脾脏和骨髓中的网状内皮细胞。到其他组织全身递送IVT mRNA的,但是,是由非有孔,非渗透血管内皮,细胞间连接而致密细胞外原纤维网络,限制靶细胞的可及位阻93(图5)。siRNA和pDNA递送方面的广泛但中等成功的努力和遇到的困难预示了对mRNA领域类似努力的期望。但是,重要的是要考虑这三个平台之间的概念差异。特别地,教训和siRNA的递送进行了改进(例如,临床验证具有优异的安全性和有效性的脂质纳米颗粒制剂)94,95和pDNA的需要决定是否这些改进可以类似地采用预先时,可以考虑mRNA传递或是否需要探索新颖的mRNA定制方法。
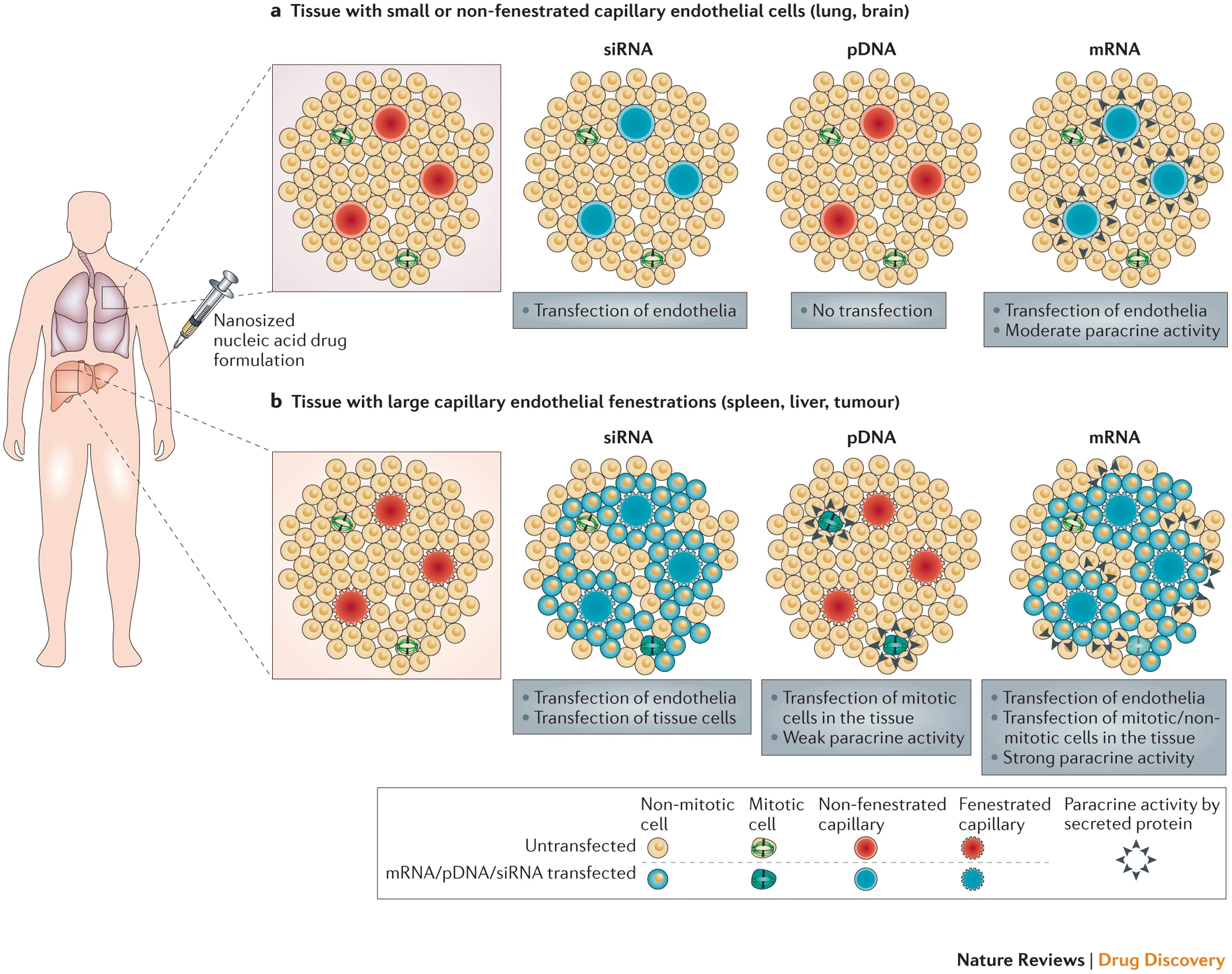
所有这三种基于核酸的药物形式均被用作纳米药物制剂,用于全身递送,并通过具有非开窗(a)或开窗(b)毛细管的毛细管系统到达器官。小干扰RNA(siRNA)的主要药理作用,即原位定义的蛋白质功能的缺失,仅限于它已进入的那些单元格。siRNA不能在由于诸如无窗毛细血管之类的生物屏障而无法直接进入的细胞中起作用。在具有内皮开窗的组织中,siRNA可能到达与毛细血管相邻的一些组织层。质粒DNA(pDNA)仅在暴露时掺入那些有丝分裂的细胞中并具有活性。这削弱了其在无开窗毛细血管的组织中的使用,并且限制了在有内皮开窗的组织中,在暴露时只有有丝分裂的组织中可转染细胞的数量。与pDNA相反,mRNA进入非有孔组织的内皮细胞并在其中起作用,在有孔组织中,mRNA到达与毛细血管相邻的细胞层中的有丝分裂和非有丝分裂细胞233。非靶细胞,例如用mRNA或pDNA转染的血管内皮细胞,可以表达药理活性蛋白,并通过旁分泌分泌,可以到达位于mRNA传递屏障234后面的靶细胞(显然,siRNA不能依靠这种功能) 。在转染的细胞中产生的蛋白质在分泌后能够扩散到靶组织中,并通过旁分泌对相邻细胞群的活性介导预期的生物学作用。这种旁分泌活性在具有无窗毛细血管的组织中可能特别有价值。
靶向细胞(例如神经元和心肌或骨骼肌细胞)尤其具有挑战性,因为它们无法直接通过系统途径递送的纳米级载体进入。因此,递送的不同的途径被测试为IVT mRNA的治疗应用在体内,如肌内,皮内,结节内,皮下,静脉内,气管内和鞘内递送4,7,9,25,26,96,97,98,99,100,101,102。用于药物递送至肺,IVT mRNA是施用气雾剂或通过肺脉管系统的静脉内定位27,103。可以通过鞘内注射到达中枢神经系统中的细胞。对于有效的癌症靶向,增强的渗透性和保留作用可能被利用,这是从正常组织与它们的解剖和病理生理学差异的实体瘤的一种独特的现象21,104。
五、临床前和临床应用
mRNA技术的进步推动了IVT mRNA在众多临床前研究和少量临床试验中的广泛治疗应用的探索(图6;表1)。目前正在研究mRNA药物的三个主要治疗领域是免疫疗法,蛋白质替代疗法和再生医学应用。
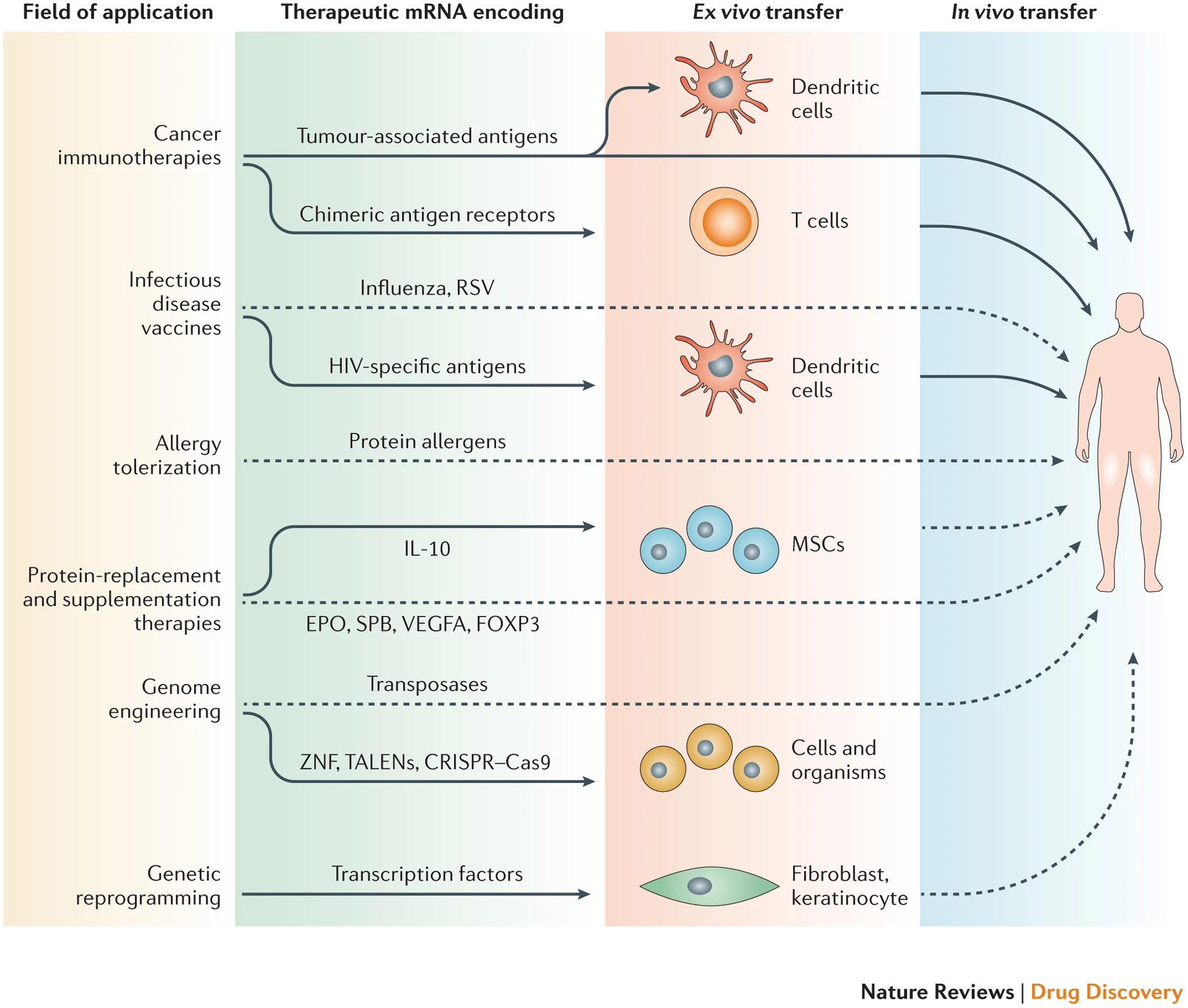
表1( https://www.nature.com/articles/nrd4278/tables/1 )详细总结了体外转录(IVT)mRNA的治疗应用。右栏中的实线箭头表示在临床中的应用,而点画箭头表示临床前的应用。Cas9,CRISPR相关蛋白9; CRISPR,成簇规则间隔的短回文重复;EPO,促红细胞生成素;FOXP3,前叉箱P3;IL-10,白介素-10;MSC,间充质干细胞;RSV,呼吸道合胞病毒;SPB,表面活性剂蛋白B;TALEN,转录激活子样效应核酸酶;VEGFA,血管内皮生长因子A;ZNF,锌指核酸酶。
5.1 癌症免疫疗法 Cancer immunotherapy
癌症免疫疗法是基于mRNA的技术在临床前和临床综合计划中进行系统探索的历史最长的领域。
在1995年,证明肌肉注射编码癌胚抗原的裸露RNA引起了抗原特异性抗体反应。一年后,证明DC暴露于编码特定抗原的mRNA或从肿瘤细胞中提取并皮下注射到荷瘤小鼠中的总mRNA会诱导T细胞免疫反应并抑制已建立肿瘤的生长。这些发现,与疫苗的目标可用性的增加由于克隆新型肿瘤抗原一起,加速了的mRNA转染的DC的方法的开发和临床平移。从那时起,使用基于众多的疫苗临床试验体外IVT基因转染的DC在癌症患者进行并由此建立了这种方法的可行性和安全性(在参考文献回顾110, 111)。
与IVT mRNA的转染的DCs治疗方案进一步细化,例如,通过优化体外DC的或由成熟共递送IVT mRNA中编码的免疫应答调节剂,例如细胞因子和共刺激因子18,112,113,114,115,116,从而提高了患者的抗肿瘤活性的87,117。同时,Argos Therapeutics已启动了一项III期临床试验,该试验使用了载有自体肿瘤衍生的扩增mRNA的DCs治疗晚期肾细胞癌患者。这项研究的数据有望在2015年发布(ClinicalTrials.gov标识符:NCT01582672)。
细胞疗法昂贵且复杂。因此,已经通过各种小组重新研究了直接体内施用编码肿瘤抗原的IVT mRNA。测试了不同的递送策略,例如阳离子脂质体和使用基因枪的轰击,取得了不同的成功(参见参考文献118)。
例如,裸露或鱼精蛋白复合物,经序列优化的IVT mRNA的皮内递送的临床试验表明,皮肤细胞发生了编码抗原的表达,并且这导致了T细胞和抗体反应的诱导9。另外,仅裸露的mRNA的皮内施用导致诱导T辅助细胞2(T H 2)型抗原特异性免疫应答。相比之下,通过共递送佐剂(例如粒细胞-巨噬细胞集落刺激因子(GM-CSF)119)或将IVT mRNA与鱼精蛋白120复合,可以实现向T H 1型应答的强烈转变。。用鱼精蛋白复合的IVT的mRNA以及mRNA的与GM-CSF结合早期临床试验表明用这些化合物即皮内注射是可行的,安全的,并可能导致抗原特异性抗体和T细胞免疫应答的诱导17,92。对该方法进行了进一步优化,从而得到了一种药物级两组分疫苗,该疫苗将裸抗原编码的mRNA与鱼精蛋白复合的mRNA佐剂结合在一起(由CureVac开发)。该疫苗在临床前研究中显示出有效的活性62,目前正在进行中的前列腺癌(ClinicalTrials.gov标识符:NCT00831467和NCT01817738)和非小细胞肺癌(ClinicalTrials.gov标识符:NCT00923312和NCT01915524)121正在进行的临床试验中进行测试。
在另一策略中,IVT mRNA被优化用于体内DC的原位转染。这种方法的目标是改善IVT mRNA的翻译和稳定性,并提高对MHC I类与mRNA编码的抗原呈递和鼠II类分子和人DCs 29,41,122,123,124。将裸露的IVT mRNA直接注射到淋巴结中被认为是诱导有效T细胞反应的最有效途径。IVT mRNA通过巨胞饮作用被淋巴结驻留DC选择性地和有效地吸收,并通过TLR7信号传导介导其成熟。所述IVT的mRNA编码的抗原和免疫刺激淋巴内环境诱导的强抗原特异性T细胞T形响应的呈现ħ 1促炎型和深刻的抗肿瘤免疫的动物模型81,97,98,125。可以通过共同施用DC激活配体FMS相关酪氨酸激酶3(FLT3)作为重组蛋白98或与所谓的TriMix共转染DC来进一步增强IVT mRNA递送后DC的免疫应答。编码免疫调节剂CD40L,CD70和截短的组成型活性TLR4的IVT mRNA的表达(参考文献99)。黑色素瘤患者的结节内裸癌IVT mRNA编码癌抗原注射的首次人体试验(由BioNTech开发)已经开始(ClinicalTrials.gov标识符:NCT01684241)。
癌症免疫治疗的个性化可通过可促进体内施用的mRNA的技术,由于其多功能性,坚固性和相对低的成本126,127,128。第一种用于治疗癌症患者的个体化疫苗的临床测试刚刚开始(ClinicalTrials.gov标识符:NCT02035956)。对来自每个入组患者的肿瘤标本进行下一代测序,并选择单个免疫原性突变以构建个性化的IVT mRNA疫苗,该疫苗编码由具有单个突变的对齐表位组成的多肽。因此,IVT mRNA可能成为根据个人基因组信息工程化的第一种药物。
除了主动免疫和免疫调节以外,IVT mRNA还被研究为免疫细胞瞬时调节的多功能工具。例如,已经通过电穿孔离体将编码肿瘤抗原特异性T细胞受体(TCR)或嵌合抗原受体(CAR)的IVT mRNA转染到T细胞或天然杀伤细胞中。带有此类mRNA编码受体的转染细胞能够识别并杀死表达靶抗原的肿瘤细胞。mRNA的瞬时性质通过过继转移的免疫细胞不受控制的扩展而降低了不良副作用的风险。编码多种抗原特异性受体的mRNA 129,130,131,132。最近,使用电穿孔了编码CARs的IVT mRNA的T细胞的细胞疗法进入了临床测试(ClinicalTrials.gov标识符:NCT01897415)。
5.2 预防传染病的疫苗
在1993年,已证明脂质体包裹的IVT mRNA编码流感病毒核蛋白可在小鼠中诱导病毒特异性T细胞应答。最近,肌内递送,自我放大用合成脂质纳米颗粒配制IVT RNA显示出在小鼠中诱导针对呼吸道合胞病毒(RSV)和流感病毒的保护性抗体应答。
当前,用于感染性疾病的三种基于IVT mRNA的疫苗方法已经进入药物开发。
为了治疗HIV感染,对高活性抗逆转录病毒疗法的患者进行免疫接种,将DC转染了编码HIV蛋白的IVT mRNA。三相I /使用不同的病毒蛋白的IVT mRNA的编码组合II期临床试验表明,该疫苗是安全和抗原特异性CD8那+和CD4 + T细胞应答可以被诱导。在其中一项研究中,离体记录了抗原特异性CD8 + T细胞对HIV抑制作用的增加;然而,在临床试验中未观察到抗病毒作用。
目前,正在使用IVT mRNA作为预防性流感疫苗的两种不同策略进行临床前研究。第一种是基于皮内注射的两组分疫苗,该疫苗含有单独或与编码神经氨酸酶的IVT mRNA结合使用的流感病毒血凝素抗原的mRNA佐剂和裸露的IVT mRNA。两种方案均可诱导针对老年和新生小鼠中相应流感病毒株的保护性免疫应答,以及对雪貂和猪的持久保护性免疫
第二种策略使用包含正链RNA病毒序列的自扩增IVT mRNA(专栏2)。最初,针对黄病毒模型开发了该策略,并且皮内递送少于1 ng IVT基因组mRNA的皮内递送可实现针对黄病毒感染的保护性免疫,这对应于减毒病毒7。基于RNA的疫苗传染病的随后的研究集中在与α病毒家族的重组RNA复制子系统136,137(在参考文献综述138,139)。其中编码结构蛋白的基因通过编码病毒抗原的基因替换RNA复制子载体已被用于引发黄病毒,RSV,流感和副流感病毒感染的动物模型的保护性抗体应答
5.3 减轻过敏的疫苗 Vaccines to alleviate allergy.
抗原特异性免疫疗法是免疫球蛋白E(IgE)介导的I型过敏性疾病的唯一治疗方式。调节T细胞反应的类型并诱导与IgE抗体竞争在变应原上的结合位点的IgG抗体是有效免疫疗法的主要作用方式。
最常见的超敏性靶抗原的分子鉴定为重组疫苗方法奠定了基础。在临床前模型,示出了基于DNA的基因疫苗以诱导T拮抗过敏机制ħ该变应原抑制特异性IgE生产1型T细胞免疫应答。但是,出于安全考虑,DNA过敏疫苗的临床翻译受到阻碍。结果表明,注射的DNA可持续2周,并且可能从注射部位扩散到全身的免疫组织和非免疫组织,因此具有引起严重过敏性副作用的潜在风险146。。在这方面,基于IVT mRNA的方法可能是有利的,因为IVT mRNA在细胞外空间会迅速降解,并且可以被改造成具有较短的细胞内半衰期。结合mRNA强大的T H 1免疫刺激能力,它可能比DNA更适合作为过敏疫苗进行开发。在诱导长期持久的变应原特异性T过敏性鼻炎,IVT mRNA的皮内注射的鼠模型抗原敏化之前ħ 1型免疫应答147,148。这些响应保护小鼠对抗过敏原特异性IgE并抑制肺部炎症的诱导由过敏原暴露介导的
5.4 蛋白质替代疗法 Protein-replacement therapies
对于基于IVT mRNA的药物,最明显的应用是补充未表达或不起作用的蛋白质,以及激活或抑制细胞途径的外源蛋白质的替代(例如治疗性抗体)。正在研究几种疾病,其中通过从转染的IVT mRNA体内产生治疗性细胞内和分泌蛋白来替代功能异常的蛋白。所有这些努力都处于开发的临床前阶段。
IVT mRNA在临床上首次用于替代有缺陷的,与生理相关的蛋白质的应用是在1992年,据报道,这是近二十年来唯一的此类工作2。该修饰的核苷可以降低RNA的免疫刺激活性的发现是在推进此应用领域枢轴75。临床前实验表明,使用核苷修饰的IVT mRNA和改进的mRNA纯化方案可消除mRNA的免疫激活并增加其翻译63,从而为蛋白质替代领域开辟了IVT mRNA的治疗应用。
在由SPB蛋白缺乏引起的先天性致命性肺疾病的小鼠模型中测试了含有修饰的核苷(2-硫尿苷和5-甲基胞苷)并编码表面活性剂蛋白B(SPB)的IVT mRNA。每周两次将SPB mRNA气雾剂递送到肺中,可保护小鼠免受呼吸衰竭的影响,并延长小鼠的平均寿命25。在小鼠和猕猴的实验中,使用了高效液相色谱法纯化并编码促红细胞生成素的伪尿苷修饰的IVT mRNA,并检测到治疗相关水平的促红细胞生成素26。在哮喘疾病模型中,气管内递送编码调节性T细胞转录因子叉头盒蛋白P3(FOXP3)的核苷修饰的mRNA,重新平衡了肺T H细胞反应,并保护了小鼠免遭变应原诱导的组织炎症和气道高反应性27。它也表明,含有IVT mRNA的直接心肌内注射和假尿苷5-甲基胞苷,和在心肌梗塞的小鼠模型中编码血管内皮生长因子A(VEGFA),改善心脏功能和增强的长期存活23。在另一项研究中,离体转染了小鼠间充质干细胞含伪尿苷的IVT mRNA编码免疫抑制性细胞因子白介素10(IL-10)和组织归巢因子P-选择蛋白糖蛋白配体1(PSGL1)和Sialyl-Lewis(x)(SLeX)。重新注射后,这些细胞归巢到发炎的组织中,并促进快速愈合
尽管取得了这些成就,但用于蛋白质替代的IVT mRNA药物的开发仍与技术挑战相关。对于基于IVT mRNA的蛋白质递送,必须考虑翻译后修饰中细胞类型特异性的差异。例如,对于糖蛋白,糖缀合物的组成未在mRNA中编码,而取决于产生该蛋白的组织类型。并非每个细胞都有适当糖基化每种蛋白质的能力,尤其是在需要高度复杂的糖基化的情况下149。翻译后修饰的另一种类型是蛋白水解加工。内切蛋白酶的加工是各种功能多肽成熟的有机组成部分,包括生长因子,细胞因子,受体,神经肽,酶,激素和血浆蛋白150。其他蛋白质需要被蛋白质转化酶明确地切割成其生物活性形式,其在细胞内发生在高尔基体和分泌颗粒151中。已鉴定出具有不同特异性和组织分布152的几种转化酶亚型。用IVT mRNA转染的细胞需要具有所需的转化酶或内切蛋白酶,以将编码的前体加工为功能性产物。
当分泌的蛋白质在异源组织中表达时,它们的分泌信号肽可能识别不佳,并且大多数蛋白质可能保留在细胞内。相对分泌信号强度相差153 ; 因此,交换天然信号肽可能会导致蛋白质分泌增加。例如,在质粒介导的促红细胞生成素在肌肉中表达的动物模型中,当用组织纤溶酶原激活剂154代替促红细胞生成素的天然信号肽时,分泌了更多的促红细胞生成素。为了达到最大效果,理想情况下,应将IVT mRNA转染到自然分泌编码蛋白的细胞中,否则可能需要优化信号肽155。
将IVT mRNA用于广泛的蛋白质置换应用,包括当前正在用重组蛋白质解决的问题以及无法使用重组蛋白质技术的那些方面,引起了极大的兴趣。考虑到可能是IVT mRNA方法潜在候选物的蛋白质的多样性,并且目前正如此探索,因此很难预测其中哪种蛋白质将最先进入临床开发。对于具有宽广的治疗窗口,低剂量活性且已经在人体内建立药代动力学和药效学认识的蛋白质,发育障碍可能较低
5.5 重编程细胞命运 Reprogramming of cell fates.
可以使用核苷修饰的IVT mRNA在体外调节细胞表型和功能。在2010年,证明包含伪尿苷和5-甲基胞嘧啶并编码Yamanaka干细胞因子的IVT mRNA可以用作安全的策略,用于有效地将细胞重编程为多能性,而不会留下转基因的残留痕迹。IVT mRNA不仅用于诱导多能性,而且还用于区分诱导性多能干细胞(iPSC)。将编码成肌细胞测定蛋白的核苷修饰的IVT mRNA引入iPSC,导致它们直接分化为肌细胞样细胞。
此后,原来的方法的几个变体已经被描述,其权利要求任一的多能干细胞或细胞命运转换的更有效的诱导158,159,204(参考文献。审查160)。具有IVT mRNA的细胞的重编程和直接分化得益于其高的体外转染效率,无基因组整合的瞬时表达以及转移复杂混合物的能力。在IVT mRNA诱导的iPSC中缺少转基因的残留表达,不仅促进了它们在疾病模型161和毒理学测试162中的利用,而且为它们在再生医学中的应用奠定了基础。163。同样,IVT mRNA转移可用于产生具有临床价值的分化细胞。
5.6 使用IVT mRNA编码的工程核酸酶进行基因组编辑 Genome editing with IVT mRNA-encoded engineered nucleases
在过去的十年中,基因组编辑已成为基因治疗的潜在替代方法。定制设计的锌指核酸酶(ZFN的),转录活化剂样效应核酸酶(TALEN)和CRISPR-Cas9(群集规则间隔的短回文重复CRISPR相关蛋白9),用于基因组的位点特异性修饰提供强大的工具164,165,166。但是,这些方法存在进行非特定编辑的风险。从基于DNA的载体翻译的编辑酶的长期存在会导致脱靶效应167。由于核酸酶仅需要很短的持续时间,因此它们从IVT mRNA瞬时表达将使这种非特异性作用最小化。编码的ZFN IVT的mRNA,TALEN的和Cas9已经成功通过破坏或整合序列施加到编辑的基因组的离体在来自不同物种的胚胎细胞(例如,小鼠,大鼠和兔)和在体内在啮齿动物中168,169,170,171,172,173,174,175。最近,通过在单细胞胚胎阶段注射编码Cas9的IVT mRNA产生了具有特定位点基因修饰的食蟹猴,从而为创建人类疾病的灵长类动物模型提供了机会176。
编码转座酶的IVT mRNA也已用于体外和体内转座子介导的稳定基因转移。例如,睡美人,piggyBac转或Tol2转座子系统的转座可以通过mRNA的注射的表达导致在哺乳动物细胞中的基因组稳定换位177和在体内在啮齿动物中178,179,180,181。
使用IVT mRNA而不是质粒表达转座酶可增加被注射细胞的存活率,因为在细胞质中注射比原核注射更为温和179。通过
方框2:自扩增mRNA Box 2: Self-amplifying mRNA
正链RNA病毒(例如小核糖核酸病毒,α病毒和黄病毒)的RNA基因组具有双重功能245。它们充当用于RNA依赖的RNA聚合酶(RDRP)即时翻译的mRNA模板,并充当由各自的RDRP复制的基因组模板。最初复制产生的负链RNA用作继续合成正链病毒基因组的模板。在感染的后期,RNA聚合酶切换到同一RNA分子的下游启动子,并开始转录编码结构病毒蛋白的带帽mRNA。1981年完成了动物RNA病毒感染性全长基因组的首次克隆(参考文献209)),并为自扩增病毒mRNA复制子的基因工程奠定了基础。此类载体怀有RDRP基因和正链RNA病毒模拟物的特性复制功能136,210,211,212,213,214,215,216。通过从cDNA模板进行体外转录,可以轻松生产复制子RNA 。的RNA病毒的结构基因是由感兴趣的异源基因,其通过一个亚基因组启动子的控制代替137,217,218,219,220。这可以通过转基因的扩增从微量转染的重组复制子RNA中实现高水平的蛋白质生产,但避免了感染性病毒的生产。细胞内复制是瞬时的,双链RNA(dsRNA)通过触发模式识别受体来诱导干扰素介导的宿主防御机制。这导致针对插入的靶分子的强抗原特异性免疫应答。因此,自扩增mRNA载体系统非常适合疫苗开发,因为它们可提供高瞬时转基因表达和固有的佐剂作用。
六、IVT mRNA的临床翻译
通过依靠患者的身体来制造所需的蛋白质,IVT mRNA药物提供了一种方法,可以稳定而可调节地生产治疗性蛋白质,而无需在发酵罐中昂贵地制造蛋白质。与这些独特功能相关联的愿景是,利用IVT mRNA将有助于应对新兴技术中的挑战,例如靶向基因组工程,干细胞的产生和重编程以及按需生产个性化疫苗。
为了充分发挥mRNA作为治疗手段的潜力,需要认真考虑有关临床和产品开发的法规(专栏3)和科学问题。
到目前为止,IVT mRNA药物的临床经验仅限于免疫治疗应用。在仅使用IVT mRNA或IVT mRNA转染的DC进行疫苗开发的临床程序中,很少有足够先进的程序可以为其他应用提供足够广泛的知识基础。对于每种应用,都必须对治疗方案的变量(例如剂量,治疗时间表和给药途径)进行完善的系统探索,以识别合适的方案。
早期临床试验的共同目标是探索药物的药代动力学特征并进行剂量发现。但是,mRNA药物的药理作用很复杂,因为IVT mRNA并不是最终的药理活性剂。迄今为止,尚未充分研究其编码的蛋白质的生物利用度是否能在临床条件下得到稳健而精确的控制,由于个体间和个体间的高变异性,这尤其具有挑战性。伴随药物也需要考虑,特别是当IVT mRNA治疗与影响mRNA代谢和翻译的其他药物(例如某些抗生素和抗癌药物)结合使用时。
其他与mRNA的复杂药理学有关的关键挑战,特别是与mRNA的递送有关的其他关键挑战涉及需要精确靶向特定细胞类型和器官的应用。
专栏3:基于mRNA的治疗药物的监管框架
现有的有关新分子实体的标准指南需要适应基于mRNA的药物。迄今为止,尚无主管当局正式声明其对mRNA药物将如何分类的一般立场,也未发布任何指导和指南。由于先例的数量有限且基于mRNA的应用广泛,因此无法预测每种单独的研究性mRNA药物,美国,欧盟和欧洲国家主管当局如何看待体外转录(IVT)mRNA。监管角度。
人们会期望将mRNA药物的分类分为生物疗法,基因疗法或体细胞疗法。
使用IVT mRNA的大多数临床试验已由欧洲团队发起,并已在欧洲进行。因此,在美国食品药品监督管理局(FDA)如何分类基于mRNA的治疗方法方面,没有很多现实生活中的例子。
FDA对基因疗法的定义如下:“ …活细胞遗传物质的修饰。可以对细胞进行离体修饰以随后施用于人,或者可以通过直接施用于受试者的基因疗法在体内改变细胞。当先对细胞进行遗传操作,然后再施用于患者时,这也是体细胞疗法的一种形式。用于转移遗传物质进行此类疗法的重组DNA材料被认为是基因疗法的组成部分。” 由于RNA不会导致“活细胞遗传物质的修饰”,因此人们可以预期,在美国,其管理不会被归类为基因疗法。
在欧盟,基于mRNA的疗法最有可能落入欧洲药物管理局(EMA)的先进疗法药物产品法规(第2009/120 / EC号指令),该法规涵盖基因疗法,工程体细胞和组织工程产品。
该法规对基因治疗药物的定义如下:“基因治疗药物是指具有以下特征的生物药物:”为了调节,修复,替换,添加或删除基因序列的人类;(b)其治疗,预防或诊断作用直接与其所含的重组核酸序列有关,或与该序列的基因表达产物有关。基因治疗药物不应包括抗传染病的疫苗。”
体内施用的mRNA药物产品被认为是符合基因治疗产品的EU定义的添加的重组核酸。一个有趣的例外是离体转染的树突状细胞给患者服用IVT mRNA之前。EMA的高级疗法委员会(CAT)并未将此类产品归类为基因疗法,因为在将其过继转移给患者时,mRNA被认为在细胞内降解。CAT将该细胞产物归类为体细胞治疗产物。此外,用于预防传染病的疫苗的mRNA药物不太可能被归类为基因疗法。根据第2001/83 / EC号指令附录I的第IV部分,基因治疗药物不包含抗传染病疫苗。此外,基因疗法的法律定义仅涉及生物医药产品。因此,通过化学方法生产的产品不符合该定义。
为基因疗法建立的指南可能为建立RNA疫苗的监管框架提供有价值的路线图。但是,与DNA和病毒载体相反,mRNA不包含启动子元件,也不整合到基因组中,除非传递编码DNA修饰酶的mRNA,否则不会发生基因破坏。mRNA表达是剂量依赖性和瞬时的。因此,没有科学合理的理由来测试IMP(研究药物)的基因组整合,种系传播,遗传毒性或致癌性,或在临床研究中对患者进行长期观察。未来的指导应考虑这些特征,因为它们在预期风险方面将mRNA产品与(其他)基因疗法区分开来。
七、安全注意事项
使用IVT mRNA进行免疫治疗的临床经验显示出极好的耐受性和安全性,并表明mRNA药物没有平台固有的主要风险。
但是,对于基于mRNA的疗法的大多数其他应用,包括基于mRNA的蛋白质替代疗法,目前尚无临床经验,这使开发人员和监管者对可能发生的安全性问题的性质和频率不确定。
与其他药物类别相关的各种安全风险不适用于基于mRNA的疗法(专栏3)。IVT mRNA的生产相对简单,制造过程以及产品质量均一且易于控制(专栏4)。不涉及细胞和动物成分,与重组蛋白相比,IVT mRNA的与过程相关的风险要低得多。
但是,必须考虑各种风险因素。
7.1 IVT mRNA介导的免疫机制激活
从安全的角度考虑,IVT mRNA的免疫激活特性是一个重要的特征,特别是对于全身给药的IVT mRNA。潜在的机制正在广泛研究中。如上所述,先天免疫系统,包括TLR3,TLR7和TLR8的几个信令受体所讨论的,已经显示出介导的mRNA诱导的免疫活化和细胞因子分泌65,66,67,183,184。在临床前研究中,干扰素-α,IL-6,肿瘤坏死因子-α和干扰素-γ诱导的蛋白10(IP-10;也称为CXCL10)被确定为通过全身IVT mRNA传递上调的关键细胞因子。免疫激活和分泌的细胞因子的概况取决于IVT mRNA的配方,包括粒径64。
在动物中进行安全性研究是可取的,但由于物种特异性差异,可能不是完全结论性的。为了补充动物研究,应在体外测试IVT mRNA制剂对人白细胞的药效。由于免疫激活是剂量依赖性的,因此建议保守剂量逐步增加,起始剂量低,并密切监测患者。未来的研究将显示核苷修饰的IVT mRNA是否会在临床环境中避免人类TLR的激活。
对于IVT mRNA作为疫苗的应用,期望瞬时免疫活化。但是,作为临床研究计划的一部分,剖析每种单独的mRNA药物的免疫修饰作用的确切性质并评估是否确实需要这一点很重要。例如,应避免186干扰素-α的诱导,这会减慢翻译机的速度。
当前数据没有表明针对IVT mRNA本身具有任何免疫原性的诱导。但是,越来越多的证据表明,患有系统性红斑狼疮和其他自身免疫性疾病的患者可以发展出抗自身RNA自身抗体,这些抗体在诱导和发展自身免疫性方面具有重要作用。因此,在某些情况下,例如长期反复全身性应用mRNA,抗RNA抗体可能会形成并介导免疫病理。人们可能会考虑筛选mRNA序列,以避免易于诱导mRNA特异性抗体的构象。因此,建议对自身免疫现象进行临床监测并进行抗核抗体实验室测试。
7.2 IVT mRNA编码蛋白的免疫原性
对于重组蛋白,众所周知的是,意外的免疫原性可能导致不良事件,例如过敏反应,细胞因子释放综合征和输注反应。此外,免疫反应可以中和蛋白药物的生物活性,以及内源性蛋白质对应物189,190,191。一个突出的实例是中和抗体,以治疗性促红细胞生成素,通过与内源性促红细胞生成素交叉反应引起猴和人的红细胞发育不全的感应192,193,194。
原则上,抗蛋白质抗体可以针对从任何IVT mRNA表达的蛋白质发展,特别是如果采用重复给药方案的话。
然而,与重组蛋白药物相反,体内产生的蛋白治疗剂是自体的,在人细胞中产生,并且可能经历正确的翻译后修饰和折叠。此外,IVT mRNA不会发生与蛋白质制造过程相关的免疫原性风险因素,例如蛋白质聚集或源自产生蛋白质的细胞或培养基的杂质。
由于大多数对治疗蛋白产品的免疫介导的不良反应是通过体液机制介导的,因此针对治疗蛋白产品的循环抗体已成为定义免疫应答的主要标准。这些应在IVT mRNA介导的蛋白质替代方法的临床研究中进行筛选。
也可以想象外源蛋白的表达以及由mRNA主链介导的促炎作用可能导致组织水平的免疫病理。对于免疫治疗方法,这可能无关紧要,因为抗原呈递细胞是mRNA传递的靶细胞,一旦它们已转变为成熟状态,它们的生命就会很短。但是,如果将其他器官(例如肝,肾,肺或心肌)作为目标,则需要解决此风险。正在进行的各种应用都使用肝脏作为靶器官,正如已经证明的(至少对于各种siRNA递送平台而言),默认情况下基于核酸的药物被路由至肝脏,因此可以实现肝脏靶向195没有进一步优化交付195。由于肝毒性可能危及生命,因此必须格外小心,并且需要测量肝酶(例如转氨酶)。但是,鉴于该器官具有独特的免疫学特性,使用肝脏作为第一代基于mRNA的蛋白质替代疗法的蛋白质表达的储库器官,甚至具有一定的风险,因为它具有诱导抗原特异性的能力。特定的耐受性可能抵消免疫原性196。
与非天然核苷酸相关的风险。高度丰富的细胞外核糖核酸酶已经进化为细胞外空间中RNA水平的强大控制机制。由于人体每天分解大量大量的天然mRNA,因此与由天然核苷酸组成的IVT mRNA药物的吸收,分布,新陈代谢和排泄特征无关,预计不会有重大风险。但是,这可能不适用于含有非天然修饰核苷酸的研究性mRNA药物。分解代谢和排泄的机制以及对多核苷酸结构中非天然核苷酸或其代谢物的其他毒性相关途径的潜在有害交叉效应以及与之相关的潜在风险仍然未知。
非天然核苷类似物用作抗病毒和抗癌药物会干扰病毒和肿瘤细胞的复制,这一发现得到了支持。许多这些核苷类似物的证明意想不到线粒体毒性198,199是与核苷转运的功能相关联200。用于治疗HIV感染患者的核苷逆转录酶抑制剂引起严重的临床毒性(例如,肌病,多发性神经病,乳酸性酸中毒,肝脂肪变性,胰腺炎和脂肪营养不良),包括由于线粒体功能障碍导致的致命并发症199。非天然修饰的核苷的这些不利影响是由DNA聚合酶γ,酶线粒体DNA复制单独负责,阻塞的抑制引起的从头线粒体DNA合成201。这些风险并没有在小鼠中进行临床前研究和大鼠鉴定由于在核苷转运蛋白1(参考文献的亚细胞定位间差异202,203)。
在临床试验设计中,应通过保守的剂量递增方案和对危险器官的仔细评估,努力解决核苷类似物的潜在毒性。安全监测必须考虑到,不良反应仅在长时间用核苷类似物治疗后才会发生。
有关编码蛋白的安全性考虑。除上述风险外,还必须考虑由编码蛋白质的性质和应用类型决定的“内容”特定风险。基因的数目和由这些基因执行的作用方式是高度不同的。因此,无法提供全面的详尽风险评估;取而代之的是,风险必须根据具体情况进行尽职调查。
取决于特定的应用,确保体内转移的RNA仅进入其预期的细胞类型可能是一项重要的安全措施。
另一个需要注意的问题是在剂量方面具有挑战性的蛋白质,例如具有狭窄治疗窗口或陡峭的剂量反应关系的蛋白质。此类蛋白质靶标的关键挑战是控制其生物利用度的稳健性和保真度,并通过密切监控,单独调整的给药时间表来解决潜在的个体间差异。
方框4:基于mRNA的治疗剂的GMP
通过体外转录产生mRNA是明确定义的程序。起始材料通常是质粒DNA载体,其包含噬菌体RNA聚合酶的启动子,编码目标蛋白质的开放阅读框,对应于非翻译区(UTR)的序列和poly(A)尾巴。用限制酶线性化质粒,该酶切割编码poly(A)尾巴的序列下游的DNA。纯化线性化质粒后,体外进行RNA聚合酶在四种核糖核苷三磷酸和化学合成的帽类似物存在下转录该信息。所有成分都可以从商业供应商处获得,它们是经过认证的,质量受控的,不含动物成分的材料。通过DNase消化除去残留的质粒DNA,并使用基于微珠的方法,沉淀或色谱法纯化体外转录(IVT)RNA。配制,无菌过滤和小瓶填充后,即可使用IVT mRNA药物。
制造过程必须使用完全不含RNase的材料进行,要求对过程中使用的所有组件和设备进行RNase污染的广泛测试。
由于IVT mRNA是在无细胞系统中产生的,因此可以轻松地对临床级材料的工艺开发和制造进行标准化。一旦建立,就可以使用相同的技术进行较小的改动,以产生几乎任何大小相似的单个IVT mRNA序列。在具有良好制造规范(GMP)的环境中进行过程转移和扩大规模与广泛的过程优化和协议验证相关。一旦完成高度标准化,就可以轻松保持批次间的可重复性。
除了进行各种过程分析外,IVT mRNA药物物质和配制药物产品的GMP释放还需要进行广泛的测试和表征。典型分析涉及身份,外观,含量,完整性,残留DNA,内毒素污染和无菌。而且,IVT mRNA被翻译成蛋白质产物的能力必须通过效能测试来验证。通常,这些测定的子集用于稳定性测试。在产品开发的早期阶段就其质量属性对产品进行表征,将有助于将来因工艺和制造变更而进行的可比性研究,从而加快产品开发速度。对这些属性的评估取决于对研究产品生物学的透彻了解。
稳定性不是问题,因为RNA在无RNase的环境中稳定,并且可以在室温下保存至少2年而不会显着降解。
一旦确定了IVT mRNA GMP的生产量,就可以在数月内经济高效地获得高纯度的合成mRNA,以提供标准的I / II期临床试验,包括制造和与释放相关的分析。取决于患者的剂量和人数,相对较小的制造工厂可能会提供早期临床测试所需的药物材料。在最近的临床试验中,每位患者17的初始剂量为600μgmRNA 16或总剂量为800μgmRNA,以实现有效的抗原特异性免疫反应。但是,必须考虑精确的量取决于所用的mRNA骨架,具体的应用类型以及IVT mRNA是离体给药还是体外给药体内。必须预料到,在需要长期或长期治疗的蛋白质替代设置中,每位患者的总剂量可能以毫克为单位。目前,每批GMP mRNA的生产能力为几克。
功能性mRNA的化学合成领域的进步可能会进一步降低生产的便利性和成本。然而,到目前为止,RNA的化学合成仅限于非常短的阅读框(少于150个核苷酸,对应于最多50个氨基酸)。
八、结论与观点
如本综述所述,癌症免疫疗法是mRNA药物生产的临床测试和工业化处于后期阶段的唯一领域。对于针对传染病的疫苗接种,IVT mRNA在早期临床测试中,而在其他所有医学应用中,例如蛋白质替代,则处于临床前阶段。
mRNA的不稳定性(最初被认为是RNA药物开发中的主要障碍)已得到有效解决。可以实现细胞内稳定性,并且通过调节mRNA翻译和mRNA代谢的结构元件将mRNA翻译活性的半衰期从数分钟调节至数天,现在已用于IVT mRNA设计。细胞外稳定性正在通过制剂的开发来解决,例如鱼精蛋白和纳米颗粒载体。IVT mRNA的去免疫技术的进步促进了在动物模型中控制mRNA的炎症活性。此外,对于mRNA药物的生物药物开发,已经奠定了有关专利和知识产权问题的初步基础(专栏5))。IVT mRNA可以以相对较低的成本在几个小时内生产,并且生产和纯化过程非常可靠,从而可以生成长度范围从数百个核苷酸到10,000多个核苷酸的mRNA。生产过程的鲁棒性和易用性促进了用于药物发现和迭代药物优化的高通量方法的实施。一旦确定了临床mRNA候选药物,就可以在几个月内进行工艺优化和临床级良好生产规范(GMP)生产。根据我们的经验,用于IVT mRNA的临床研究GMP批次的生产成本平均比在真核细胞中生产的重组蛋白疗法低五至十倍。
为此满意的解决方案仍然悬而未决,特别是对于主要挑战非免疫治疗相关的体内应用中,定位到期望的器官或细胞类型的体内和IVT mRNA的复杂药理学。这意味着跨组织和患者一致剂量的问题可能成为体内施用IVT mRNA的临床发展的重要障碍。如上所述,仍不清楚如何将IVT mRNA准确地递送至靶细胞类型以及如何达到正确的治疗剂量水平。此外,在比较独立的给药途径时,mRNA剂量-蛋白质-效应关系是个体间还是个体内变化,尚未得到彻底研究。
在这方面,离体转染细胞的用途具有IVT mRNA的蛋白,特别是用于免疫治疗方法的蛋白,可以被视为“垂头丧气的果实”。对于免疫疗法,编码相应抗原的相对少量的IVT mRNA足以获得可靠的功效信号,这进一步受到mRNA固有的佐剂活性的支持。而且,作为基于mRNA的疫苗递送目标的专业抗原呈递细胞组成性地配备有专门的mRNA摄取机制。除了用于癌症免疫疗法的应用之外,基于mRNA的疫苗开发还可能为管理新出现的大流行病创造机会。合成DNA技术的最新进展使得能够快速,准确地合成编码任何潜在靶抗原的基因205。快速组装的合成基因的大规模生产是适合体外转录的合适的DNA模板,可以加速基于mRNA的疫苗生产的整个过程。
当将IVT mRNA治疗药物扩展到诸如蛋白质替代疗法,给药的剂量,剂量和稳健性以及体内施用的mRNA药物的组织选择性等应用时,需要仔细解决。而且,免疫刺激是不需要的。结果,推进非免疫疗法应用的障碍更高,并且其通过来自免疫疗法领域的溢出效应的加速是有限的。对于许多蛋白质替代疗法应用而言,可以通过优化现有的递送工具来成功实现IVT mRNA的递送。最合理的方法是选择目标组织易于接近且编码的蛋白质即使在低剂量下仍具有活性且具有宽广的治疗窗口的疾病。
为了将mRNA开发为生物药物,mRNA技术平台必须成为行业兼容的过程。对于在细胞治疗应用中离体使用的IVT mRNA ,这将受到细胞治疗206面临的具有挑战性的工业化障碍的限制。体内IVT mRNA相比之下,在一般药物特性方面,药物的使用遵循“平台”特定的模式,并且其制造简单,成本效益高,并且没有特定的挑战。进度还将取决于流程自动化的发展方式以及专业公司是否可以为此目的提供标准或定制设备。对于寻求外包制造的基于产品的公司,服务提供商数量少会阻碍项目计划和时间表。围绕核心mRNA药物产品的服务和供应行业的多元化格局已经开始发展,并将促进工业化。
在基因治疗和siRNA相邻领域的失望和失败的阴影下,mRNA领域已得到谨慎发展。避免了主要错误,例如过早采用新技术,具有不必要安全风险的临床试验以及行业领导者和投资者的不切实际期望。在充分的临床前探索和对潜在机制的了解的基础上,已经启动了正在进行的临床测试计划。建议进一步保持这种审慎性。
方框5:专利与知识产权格局
在过去的10年中,基于mRNA的治疗技术的核心领域的专利申请数量已大大增加。与mRNA相关的主要知识产权类别是“物质组成”专利和与mRNA本身相关的申请,涉及mRNA传递配方的申请以及某些应用中要求mRNA的专利。相对于小干扰RNA(siRNA)领域,药物格式本身的治疗用途已获得基本专利221的限制,没有基本专利限制了体外的广泛工业应用转录(IVT)mRNA用于治疗。当前的专利格局的特点是碎片化程度低。目前可见的最高专利活动来自专门研究基于mRNA的疗法的一小撮生物技术公司。这些专利组合记录了开发这些公司各自的知识产权的预期系统性和战略性方法,以此作为每个公司业务模式的基础。越来越多的专利申请来自具有临床前研究成果的学术团体,以及来自行业的使用IVT mRNA替代已确定的疾病靶标的行业。
由于该领域还很年轻,因此尚未批准许多专利申请。
参考资料
- Ugur Sahin, Katalin Karikó and Özlem Türeci.mRNA-based therapeutics — developing a new class of drugs.Nature Reviews Drug Discovery. 2014,19 September, doi:10.1038/nrd4278 。 https://www.nature.com/articles/nrd4278
